Hoe ontstaan chronische klachten bij patiënten met fibromyalgie? De insula, een hersengebied met een mogelijke sleutelrol
Hoe ontstaan chronische klachten bij patiënten met fibromyalgie?
De insula, een hersengebied met een mogelijke sleutelrol
- Wanneer pijn chronisch wordt, is de pijnperceptie buiten proportie en kan deze niet meer volledig toegeschreven worden aan somatische of neuropatische processen.
- Patiënten met fibromyalgie gaan gebukt onder chronische pijn en diverse lichamelijke en psychosociale stoornissen.
- Een overdreven glutamaateffect (stimulerende activiteit) in het insulagebied kan het uitgebreide symptomencomplex verklaren.
- Herstel van de glutamaat-GABA-balans in de insula is mogelijk via antagonisten van de glutamaatreceptor en door hersenstimulatie.
- Cognitieve gedragstherapie en fysieke activiteit hebben vergelijkbare positieve effecten.
Inleiding
In Europa lijdt één op vijf personen aan chronische pijn, die zich kan lokaliseren in een specifieke regio, maar ook over het hele lichaam kan voorkomen zoals het geval is bij fibromyalgie. Eén op twintig personen kampt met fibromyalgie en ervaart chronische wijdverspreide spierpijnen en spierstijfheid. Maar histologisch onderzoek van spierweefsel toont geen beschadiging of degeneratie. Aangezien de oorzaak van deze spierklachten en pijnen niet gevonden kan worden in de periferie, dient deze gezocht te worden in het centraal zenuwstelsel waar de pijnsignalen worden verwerkt. Een complex samenspel van autonome en neuro-endocrine processen beïnvloeden de pijnverwerking in het centraal zenuwstelsel.
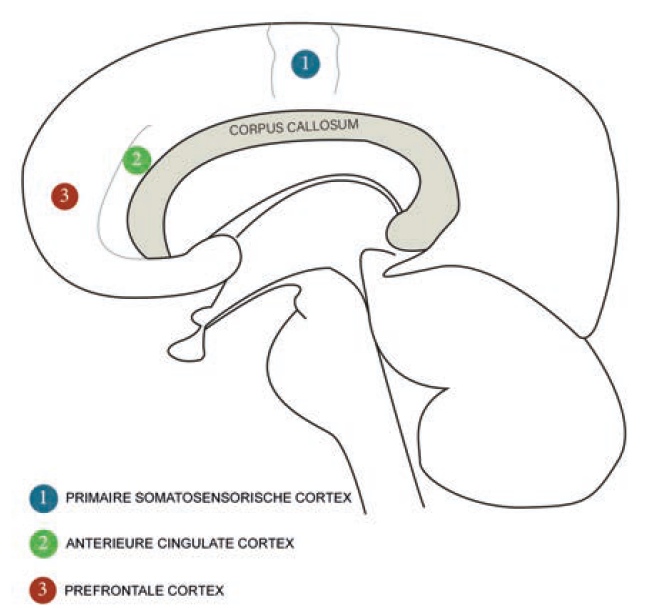
De insula, een hersenregio diep verscholen in de laterale sulcus, is één van de belangrijkste hersengebieden verantwoordelijk voor de pijnperceptie (figuur 1).1 Deze hersenregio verwerkt niet enkel sensorische informatie (waar komt de pijnprikkel vandaan, wat voor type is dit en hoe bedreigend), maar bepaalt mee hoe we reageren op de pijnprikkel (hoe we denken over de binnenkomende pijn, welke emoties opkomen en hoe we ons daarnaar gedragen).
De vier functioneel verschillende regio’s van de insula zijn weergegeven in figuur 1. Ze reageren op een brede waaier van stimuli. Deze zijn: 1) een sensorimotorische regio, gelegen in de mid-posterieure insula; 2) een centraal-olfactogustatoire regio; 3) een socio-emotionele regio in de anterieur-ventrale insula; en 4) een cognitieve anteriodorsale regio.2
Figuur 1: Doorsnede van de hersenen met daarop de anatomische regio’s betrokken in het pijnproces. Bovenaan de mid-sagittale doorsnede en onderaan de coronale doorsnede.

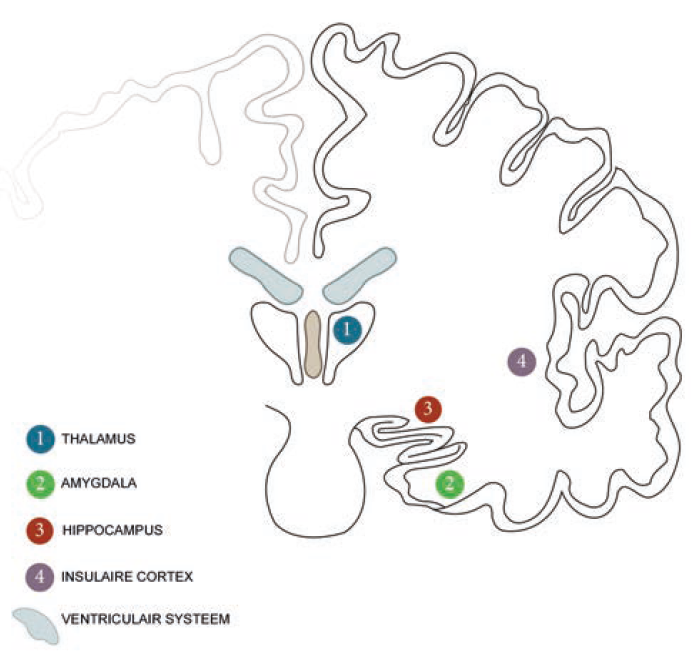
De posterieure insula zou instaan voor het analyseren van sensorische pijnsensaties, terwijl de anterieure insula in verband wordt gebracht met het verwerken van subjectieve, pijngeassocieerde gevoelens. Het is eerder al aangetoond dat bij een verhoogde pijngevoeligheid, zoals bij fibromyalgie, het brein, en meer bepaald de insula, zich functioneel en anatomisch aanpast.
Onderzoeksvraag
Naast de spierpijn ervaren patiënten met fibromyalgie ook heel wat andere klachten in verscheidene regio’s van het lichaam. Tot op heden is er nog geen consensus over het onderliggende mechanisme en daarom krijgen patiënten vaak te kampen met onbegrip en worden ze niet adequaat behandeld.
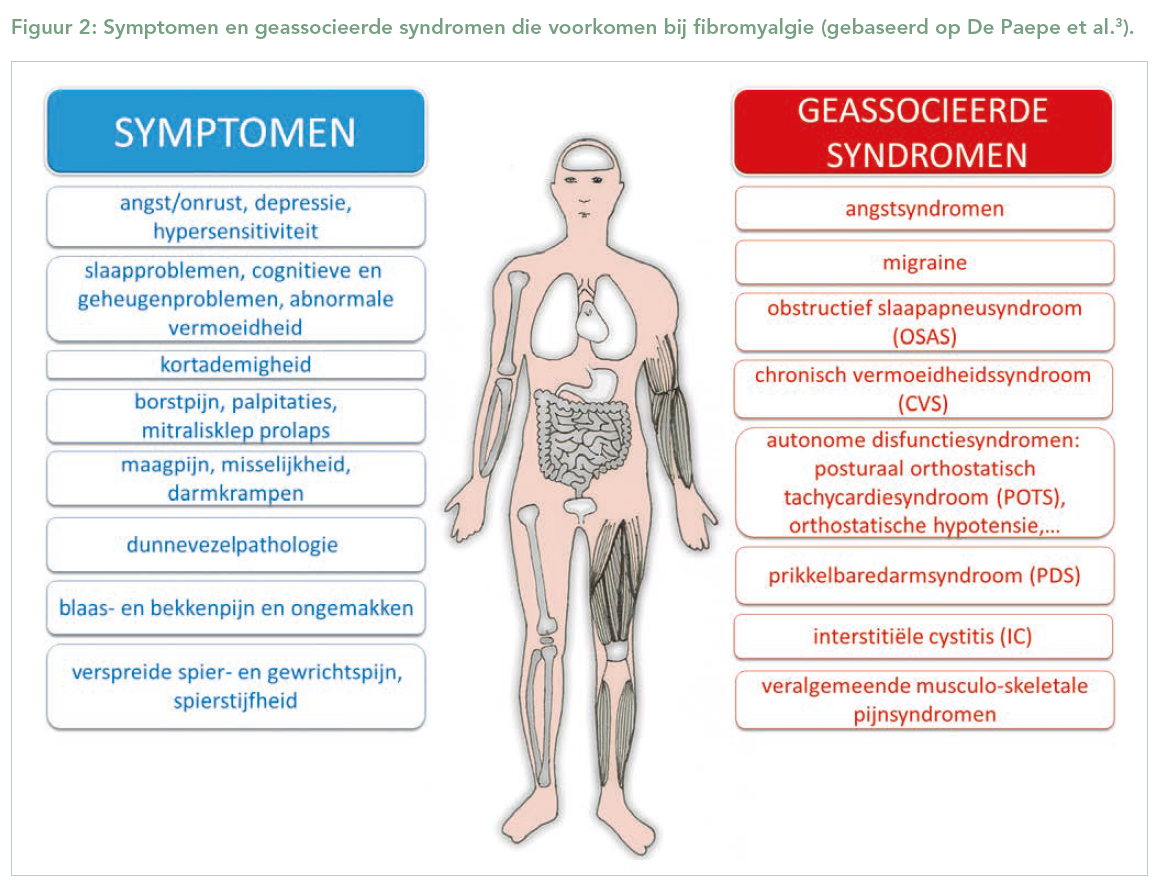
Dit motiveerde ons om een multidisciplinair team van experten samen te stellen, wiens gezamenlijke inspanningen geleid hebben tot een nieuwe hypothese over het mechanisme van fibromyalgie, waarin de insula een sleutelrol speelt.3 Meer specifiek concludeerden we op basis van het samenbrengen van de resultaten uit verschillende studies dat de balans tussen de exciterende of werkingsstimulerende neurotransmitter (glutamaat) en de inhiberende of werkingsremmende neurotransmitter (gamma-aminoboterzuur, GABA) ter hoogte van de insula de pijnverwerking ontregeld is. Deze hypothese biedt niet alleen een verklaring voor de spierpijnklachten, maar eveneens voor verscheidene andere klachten en syndromen die vaak met fibromyalgie gepaard gaan, waaronder blaaspijn, prikkelbaredarmsyndroom, obstructieve slaapapneu, chronische vermoeidheid en autonome disfunctie (figuur 2).
Hoe de insula het klachtencomplex beïnvloedt
Pijnklachten
De neurotransmitter glutamaat zorgt voor sensitisatie of overgevoeligheid van het centraal zenuwstelsel. De concentratie glutamaat in pijngerelateerde hersengebieden is positief gecorreleerd aan de pijngevoeligheid van een individu. In de posterieure insula van gezonde vrijwilligers is de pijnintensiteit (geïnduceerd door een pinprik) negatief gecorreleerd met de hoeveelheid GABA en positief met de hoeveelheid glutamaat. Hoe minder GABA en hoe meer glutamaat, hoe intenser de pijn gevoeld wordt.
Bij patiënten met fibromyalgie blijkt glutamaat, samen met glutamine (de bouwstof van glutamaat), in de insula in hogere mate aanwezig te zijn in vergelijking met gezonde personen, wat resulteert in een hogere pijnsensitiviteit en dus lagere pijndrempels. Verstoringen in het GABA-metabolisme en glutamaat-turnover spelen mogelijk een belangrijke rol in het symptomencomplex bij fibromyalgie.
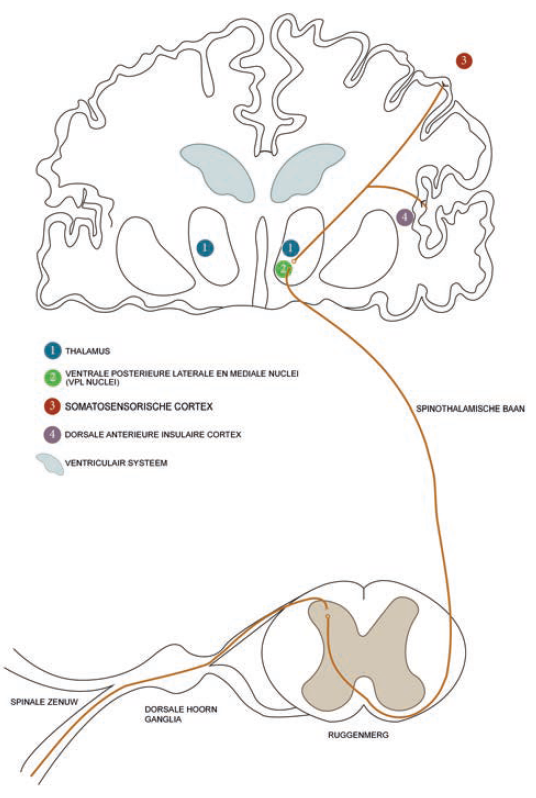
Naast deze biochemische disbalans in de insula toont MRI-onderzoek bij patiënten met fibromyalgie ook een verandering in de hersenactiviteit en connectiviteit met andere regio’s betrokken in de pijnverwerking: de dorsolaterale prefrontale cortex, de anterieure cingulate cortex, de amygdala en de hippocampus (figuur 1). De connectiviteit tussen verschillende hersenregio’s en informatie-uitwisseling tussen het centraal en perifeer zenuwstelsel is afgebeeld in figuur 3.
Figuur 3: Schematische schets van de primaire somatosensore baan. De perifere zenuw schakelt in het dorsale gedeelte van het ruggenmerg. Vervolgens verloopt het opstijgende axon via de spinothalamische baan naar de thalamus en schakelt in de VPL-kern van de thalamus met projecties naar de primaire somatosensorische cortex en naar de insulaire cortex.
Cardiovasculaire symptomen
Corticale regio’s, zoals de mediale prefrontale cortex, de anterieure cingulate cortex en de insula cortex zijn betrokken bij de regulatie van hartslag en bloeddruk. Schade aan de insulaire cortex is geassocieerd met aritmie, verstoorde diurnale bloeddrukvariatie en diverse myocardiale aandoeningen, zoals een mitralisklepprolaps die 30% vaker voorkomt bij patiënten met fibromyalgie, vergeleken met de algemene populatie.
Bij patiënten is er ook vaak sprake van autonome disfunctie, wat leidt tot onregelmatige hartslag, verminderde hartslagvariabiliteit en orthostatische intolerantie (posturaal tachycardiesyndroom of orthostatische hypotensie). Het autonoom zenuwstelsel van patiënten met fibromyalgie vertoont een dominante activiteit van de orthosympathische tak en een gereduceerde reactiviteit van de parasympatische met een overactieve reactie als gevolg op stressoren zoals fysiologische stress door een fysieke of mentale inspanning.
Blaas- en darmklachten
Het verwerken van signalen vanuit de blaas gebeurt in een netwerk van hersengebieden, waaronder de thalamus, prefrontale cortex én ook de insula die ons alert maakt over de vulling van de blaas. Patiënten met fibromyalgie hebben vaak te kampen met blaas- en bekkenbodemproblemen, zoals een toegenomen frequentie of urgentie.
Ook gastro-enterologische aandoeningen, zoals het prikkelbaredarmsyndroom, worden frequent vastgesteld bij patiënten met fibromyalgie. Communicatie tussen het brein en de darmen verloopt via verschillende systemen zoals de hersencortex, hypothalamus, hypofyse- en bijnierklieren. Deze structuren hangen nauw samen, hetzij via het perifeer zenuwstelsel, hetzij door neurohumorale stimuli. De neurotransmitter glutamaat speelt een rol in de communicatie tussen hersenen en darmen. De zogenaamde hersen-darm-as verzendt vanuit het centraal zenuwstelsel signalen om darmsecretie en -motiliteit correct te laten verlopen.
Een verhoogde concentratie van glutamaat kan gepaard gaan met het prikkelbaredarmsyndroom en is geassocieerd met een toegenomen dikte van de posterieure insula. Maar ook andere klachten zoals gastro-oesofageale reflux en maagzuur-hypersecretie kunnen een gevolg zijn van een verstoorde neurotransmitterregulatie ter hoogte van de hersen-darm-as.
Angst en depressie
Veerkracht is een belangrijke factor voor het psychologische welzijn en komt tot stand door een wisselwerking tussen cognitieve en emotionele ervaringen. Bij deze processen lijkt de insula nauw betrokken. Beeldvorming via PET/MRI op emotionele stimuli tonen de betrokkenheid van de insula, samen met andere hersengebieden, bij depressie en humeur- of angststoornissen.
Depressie en angst komen frequent voor in de context van chronische pijn en het is dan ook niet verrassend dat meer dan 30% van de patiënten met fibromyalgie angst of gemoedstoornissen ervaart. Stressvolle gebeurtenissen kunnen een uitlokkende factor vormen voor het ontstaan van fibromyalgie en ze kunnen ook leiden tot symptomenexacerbaties bij patiënten met gekende fibromyalgie.
Vermoeidheid en gestoorde slaap
Patiënten met fibromyalgie klagen frequent over een onverkwikkende slaap, slechte slaapkwaliteit, obstructieve slaapapneu (komt voor bij 45% van de patiënten) en ook vermoeidheid overdag.
Gestoorde slaap en vermoeidheid zijn gelinkt aan autonome disfunctie en/of veranderingen in de insula. Polysomnografie toont aan dat patiënten met fibromyalgie een gereduceerde tragegolfslaap en abnormale alfaritmes vertonen, wat suggestief is voor waakzaamheid tijdens niet-REM-slaap. Patiënten rapporteren afgenomen slaapkwaliteit en ervaren ergere pijnsymptomen wanneer ze slecht slapen.
De vermoeidheidsklachten kunnen slechts gedeeltelijk verklaard worden door een slechte slaapkwaliteit en zouden gerelateerd kunnen zijn aan een verstoorde functie van de insula. Zo toonde onderzoek bij patiënten met reumatoïde artritis, een aandoening waarbij zowel pijn als vermoeidheid belangrijke symptomen zijn, een verhoogde connectiviteit in de linker insulaire regio. Ook werd reeds aangetoond dat bij mensen die obstructieve slaapapneu vertonen, er minder GABA en meer glutamaat aanwezig is in de insulaire cortex en deze ongepast reageert op autonome gebeurtenissen.
Dunnevezelpathologie
Dunnevezelpathologie verwijst naar schade aan de kleine, meestal ongemyelineerde zenuwvezels die door onze huid, perifere zenuwen en organen lopen, en komt zeer frequent (45-69%) voor bij personen met fibromyalgie.4 Deze aandoening kan worden vastgesteld via huidbiopsie of corneale confocale microscopie (een pijnloze procedure waarbij optische sneden doorheen de cornea worden gemaakt om aantal en lengte van zenuwbundels te evalueren) en kan leiden tot pijn, tintelingen, gevoelsstoornissen, enzovoort.
Dunnevezelpathologie is niet hetzelfde als dunnevezelneuropathie (gekend bij patiënten met diabetes); het verschil tussen beide entiteiten is bij patiënten met fibromyalgie duidelijk te onderscheiden. Wanneer in de insula bij ratten glutamaat kunstmatig wordt verhoogd, leidt dit tot een afname van de densiteit van ongemyelineerde zenuwvezels, resulterend in een verhoogde pijngevoeligheid bij deze proefdieren, wat sterk overeenkomt met de symptomen bij patiënten met fibromyalgie.
De insula als behandeldoelwit
Nieuwe diagnostische test- en behandelstrategieën
Het ziektemechanisme van fibromyalgie wordt beter begrepen, wat aanleiding geeft tot diagnostische en therapeutische vooruitgang. Er is nu voor het eerst een ‘positieve’ diagnostische test ter beschikking van fibromyalgiepatiënten, namelijk de opsporing voor dunnevezelpathologie via een huidbiopsie die positief is bij 60% van de patiënten met fibromyalgie.
Ook via specifieke functionele beeldvorming van de hersenen (functionele MRI) kunnen veranderingen in de glutamaat-GABA-balans gedetecteerd worden, maar het is nog wachten tot dit type beeldvorming ook voor klinische toepassing beschikbaar wordt. Deze nieuwe mechanistische inzichten hebben geleid tot de ontwikkeling van nieuwe behandelstrategieën voor fibromyalgie (figuur 4).
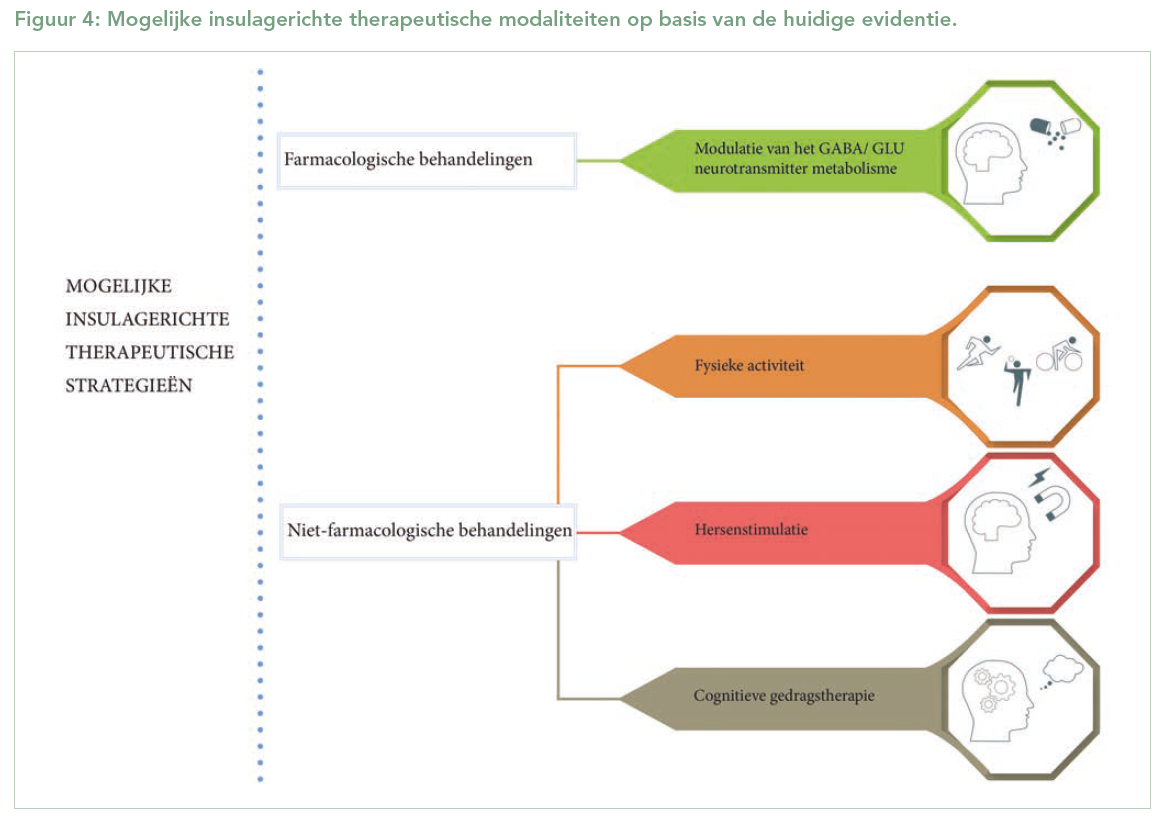
Farmacologische behandeling
Modulatie van het aantal glutamaatreceptoren of hun reactiviteit, via het blokkeren van de receptor door antagonisten, heeft therapeutisch potentieel voor chronische pijn van verschillende origines.
De belangrijkste glutamaatreceptoren worden biochemisch onderverdeeld in ionotrope (gekoppeld aan een ion-kanaal) receptoren die snelle synaptische reacties mediëren en metabotrope of G-eiwit gekoppelde receptoren die een langzamere neuromodulerende werkingen hebben. Ionotrope n-methyl-d-aspartaat (NMDA)-receptoren bevinden zich in het postsynaptische membraan van neuronen en zijn essentieel voor het verwerken van leer- en geheugenopdrachten. Activatie van de NMDA-receptor resulteert in verhoogde sensitiviteit voor sensorische informatie. Metabotrope receptoren zijn meer wijdverspreid en moduleren neuronale activiteit.
NMDA-receptorantagonisten
Bij patiënten met fibromyalgie is de activiteit van NMDA-receptoren verhoogd, waardoor ze een mogelijk doelwit zijn voor therapeutische interventies met antagonisten van de receptor.
Ketamine zorgde in een pilootstudie bij patiënten met een ‘complex regionaal pijn syndroom type 1’ (dit is het type zonder zenuwschade) voor een belangrijke pijnverlichting waarbij de psychomimetische bijwerkingen (hallucinaties bijvoorbeeld) acceptabel waren.5 Dit weliswaar zonder dat een verbetering van het dagelijks functioneren kon worden vastgesteld.
Andere NMDA-receptorantagonisten, zoals dextromethorphan en memantine kunnen positieve effecten hebben bij pijnsyndromen. Actueel wordt in klinische studies nagegaan of een nieuwe klasse van antagonisten, NYX-2925 genaamd, gebruikt kan worden om de pijnklachten te reduceren.
Metabotrope glutamaatreceptoren
Een alternatieve strategie bestaat uit het toedienen van antagonisten van de metabotrope glutamaatreceptoren die verantwoordelijk zijn voor de trage neuromodulaire respons.
Toenemende wetenschappelijke evidentie wijst erop dat deze receptoren betrokken zijn in diverse psychiatrische ziekten en mogelijk ook bij patiënten met fibromyalgie, want majeure depressie komt voor bij 20-40% van de patiënten.
GABA-derivaten
GABA-derivaten worden frequent voorgeschreven om pijn te verlichten. Zo zijn gabapentine en pregabaline doeltreffend om pijnlijke diabetische neuropathie en postherpetische neuralgie te verlichten.
Twee meta-analyses concludeerden dat pregabaline de pijn van patiënten met fibromyalgie significant verminderde en de slaapkwaliteit verbeterde; ook de algemene levenskwaliteit ging erop vooruit.6,7 Pregabaline inhibeert de presynaptische vrijstelling van exciterende neurotransmitters door de alfa2delta-calciumkanalen te blokkeren. Hierbij wordt wellicht de vrijstelling van glutamaat in de synaptische spleet verminderd. Meer specifiek daalden de gecombineerde glutamaat/glutamineniveaus binnen de posterieure insula wanneer patiënten met fibromyalgie pregabaline gebruikten.
Niet-farmacologische behandeling
Hersenstimulatie
Hersenstimulatie als behandeling wordt reeds enige tijd overwogen. De wetenschappelijke literatuur beschrijft een pijnverlichtend effect, maar het klinisch potentieel blijft omstreden. Het arsenaal groeit echter gestaag en het vooruitzicht op technieken zoals niet-invasieve Transcraniële Magnetische Stimulatie (TMS) en transcraniële directe stroomstimulatie (transcranial Direct Current Stimulation; tDCS) ter behandeling van pijnaandoeningen biedt nieuwe mogelijkheden.
Bij Transcraniële Magnetische Stimulatie (TMS) wordt de elektrische activiteit van specifieke hersengebieden indirect gestimuleerd via polariteitsveranderingen in magnetische velden. Bij transcranial Direct Current Stimulation (tDCS) wordt de hersenenactiviteit gemoduleerd via elektroden die in direct contact staan met de hoofdhuid. Anodale stimulatie resulteert doorgaans in corticale exciteerbaarheid, terwijl kathodale stimulatie een corticale inhibitie tot gevolg zou hebben.
Repetitieve TMS (rTMS) met als doelwit de primaire motor cortex (M1) kan een positief effect hebben op neuropatische pijn en op gerelateerde pijnklachten bij patiënten met fibromyalgie. Een meta-analyse demonstreerde significant gunstige effecten voor rTMS, waarbij werd gesuggereerd dat M1-stimulatie een beter pijnstillend effect heeft en stimulatie van de dorsolaterale prefrontale cortex met hoogfrequente rTMS een beter antidepressief effect.8 Door sterke betrokkenheid in pijnbeleving zou de insula een goed alternatief doelgebied kunnen zijn voor dergelijke stimulatie; verder onderzoek is dus nodig naar deze potentiële behandelstrategie.
Cognitieve gedragstherapie
Cognitieve gedragstherapie leidt tot een reductie van de pijn bij patiënten met fibromyalgie, verbetert het functioneren en reduceert de emotionele stress. Aan het eind van de behandeling en op zes maanden follow-up bleek cognitieve gedragstherapie even effectief als de aanbevolen farmacologische therapieën met pregabaline en/of duloxetine, met uitzondering van het copinggedrag waarvoor cognitieve gedragstherapie superieur was.
Cognitieve gedragstherapie lijkt in staat om de disfunctionele staat van het brein en pijngerelateerde beperkingen te verminderen, hetgeen gedeeltelijk een gevolg is van een reductie in pijncatastroferen. Onder pijncatastroferen verstaan we een overdreven negatieve houding (piekeren, zich hulpeloos voelen, de pijn uitvergroten) tegenover pijn; de pijn wordt door de catastrofeerder als extreem bedreigend en leidend tot catastrofale gevolgen geacht.
In een groep patiënten met fibromyalgie die cognitieve gedragstherapie volgden, werd een substantiële vermindering van de verbindingen tussen de insula en de primaire somatosensorische cortex vastgesteld. Cognitieve gedragstherapie heeft het vermogen om katastroferen te reduceren en om de connectiviteit te normaliseren tussen ‘salience’ of ‘opvallendheidsnetwerk’ (verantwoordelijk voor het bepalen aan welke omgevingsstimuli we aandacht geven) en andere gebieden zoals de insulaire cortex en primaire somatosensorische regio’s.9
Fysieke activiteit
De positieve effecten van fysieke activiteit voor patiënten met fibromyalgie zijn duidelijk aangetoond en kunnen mechanistisch gedeeltelijk worden toegeschreven aan het herstel van de hersenconnectiviteit (neurale connecties tussen verschillende hersenregio’s) in rusttoestand.
Na drie maanden van regelmatige fysieke activiteit was er vooral een toename in de verbindingen tussen de rechter insula en de primaire sensomotorische cortex. Deze resultaten suggereren een herstel van de fibromyalgie-geassocieerde hyperconnectiviteit tussen hersengebieden betrokken in de pijnperceptie, zoals de anterieure insula en de sensomotorische regio’s. Ook werd aangetoond dat regelmatige fysieke activiteit de fosforylatie van ionenkanalen in de NMDA-receptor tegengaat, waardoor deze receptor minder reageert op prikkeling door glutamaat en de aanwezige hyperalgesie doet afnemen.10
De wetenschappelijke evidentie toont duidelijk aan dat aerobe inspanningen, maar ook krachttraining een gunstig effect hebben op het globale welzijn en functioneren van patiënten met fibromyalgie, met pijnverlichting en toename van de levenskwaliteit tot gevolg.
Wanneer pijn chronisch wordt, is de pijnperceptie buiten proportie en kan deze niet meer volledig toegeschreven worden aan somatische of neuropatische processen. Er is toenemend bewijs dat verstoringen in de glutamaat-GABA-balans in de insula bijdragen tot pijnbeleving, maar ook kan leiden tot andere fibromyalgiegerelateerde symptomen, zoals orthostatische hypertensie, blaas- en darmproblemen, angst, depressie en vermoeidheid.
Therapieën die het onevenwicht van neurotransmitters ter hoogte van de insula aanpakken of die de hersenwerking ter hoogte van insula trachten te normaliseren, door het toepassen van specifieke hersenstimulatie, zijn in volle ontwikkeling en lijken veelbelovend.
Bovendien is aangetoond dat cognitieve gedragstherapie en regelmatige fysieke activiteit kunnen leiden tot positieve hersenveranderingen en het voorkomen van overgevoeligheid van receptoren voor de neurotransmitter glutamaat.
- Starr CJ, Sawaki L, Wittenberg GFR. Roles of the insular cortex in the modulation of pain: insights from brain lesions. J Neurosci 2009;29:2684-94.
- Kurth F, Zilles K, Fox PT, Laird AR, Eickhoff SB. A link between the systems: functional differentiation and integration within the human insula revealed by meta-analysis. Brain Struct Funct 2010;214:519-34.
- De Paepe B, Smet J, Baeken C, Van Oosterwijck J, Meeus M. A capital role for the brain’s insula in the diverse fibromyalgia-associated symptoms. Med Hypotheses 2020;143:110077. Doi: 10.1016/j.mehy.2020.110077.
- Grayston R, Czanner G, Elhadd K, Goebel A, Frank B, Üçeyler N, Malik RA, Alam U. A systematic review and meta-analysis of the prevalence of small fiber pathology in fibromyalgia: Implications for a new paradigm in fibromyalgia etiopathogenesis. Semin Arthritis Rheum 2019;48:933-40.
- Sigtermans MJ, van Hilten JJ, Bauer MC, et al. Ketamine produces effective and long-term pain relief in patients with complex regional pain syndrome type 1. Pain 2009;145:304-11.
- Häuser W, Bernardy K, Uçeyler N, Sommer C. Treatment of fibromyalgia syndrome with gabapentin and pregabalin. A meta-analysis of randomized controlled trials. Pain 2009;145:69-81.
- Straube S, Derry S, Moore RA, McQuay HJ. Pregabalin in fibromyalgia: meta-analysis of efficacy and safety from company clinical trial reports. Rheumatology 2010;49:706-15.
- Lefaucheur JP, Aleman A, Baeken C, Benninger DH, Brunelin J, Di Lazzaro V, et al. Evidence-based guidelines on the therapeutic use of repetitive transcranial magnetic stimulation (rTMS): An update (2014 – 2018). Clin Neurophysiol 2020;131:474-528.
- Lazaridou A, Kim J, Cahalan CM, et al. Effects of cognitive-behavioral therapy (CBT) on brain connectivity supporting catastrophizing in fibromyalgia. Clin J Pain 2017;33:215-21.
- Andrade A, Dominski FH, Sieczkowska SM. What we already know about the effects of exercise in patients with fibromyalgia: an umbrella review. Semin Arthritis Rheum 2020;S0049-0172(20)30022-6.
- Boel De Paepe is verbonden aan de Vakgroep Inwendige Ziekten en Pediatrie, UGent en het Neuromusculair Referentiecentrum, UZ Gent;
- Joél Smet is verbonden aan de Vakgroep Inwendige Ziekten en Pediatrie, UGent;
- Chris Baeken is verbonden aan de Vakgroep Hoofd en Huid, UGent, de Dienst Psychiatrie, UZ Gent en de Dienst Psychiatrie, UZ Brussel;
- Mira Meeus is verbonden aan de Vakgroep Revalidatiewetenschappen, UGent, MOVANT, Vakgroep Revalidatiewetenschappen en Kinesitherapie, UAntwerpen en Pain in Motion, Internationale Onderzoeksgroep;
- Indra De Greef is verbonden aan de Vakgroep Revalidatiewetenschappen, UGent;
- Arnaud Vanlander is verbonden aan de Vakgroep Inwendige Ziekten en Pediatrie, UGent;
- Jessica Van Oosterwijck is verbonden aan de Vakgroep Revalidatiewetenschappen, UGent, MOVANT, Vakgroep Revalidatiewetenschappen en Kinesitherapie, UAntwerpen, Pain in Motion, Internationale Onderzoeksgroep, en het Fonds Wetenschappelijk Onderzoek – Vlaanderen (FWO).
Citeer dit artikel
De Paepe B, Smet J, Baeken C, Meeus M, De Greef I, Vanlander A, Van Oosterwijck J. Hoe ontstaan chronische klachten bij patiënten met fibromyalgie? De insula, een hersengebied met een mogelijke sleutelrol. Huisarts Nu 2021;50:84-90.